Ricerca
Proteomica tissutale
|
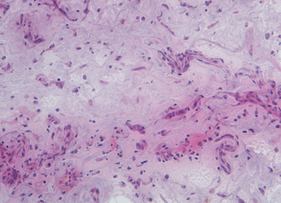
Il protocollo sviluppato per l’analisi proteomica direttamente su tessuto permette di effettuare la digestione in situ, rispettando l’istologia del tessuto stesso. Il core di tale metodica riguarda l’utilizzo di un micro-sistema versatile chiamato hydrogel che assume la forma di un disco costruito con diametro variabile a seconda delle necessità (e.g., 3 mm); tale disco contiene, tra gli altri reagenti, l’enzima per la digestione delle proteine. Posizionando il disco in specifiche aree della superficie tissutale, è possibile confinare la digestione ad una o più aree di interesse istologico. Dunque, da una singola sezione di tessuto si ottengono informazioni molecolari strettamente correlate ad ogni specifica micro-regione dove l’hydrogel viene posizionato. Tale approccio permette non solo di valutare l’espressione delle proteine di due o più regioni di una singola sezione di tessuto (e.g., area tumorale vs. aree adiacenti non tumorali), ma anche di più sezioni di tessuto diverse provenienti da pazienti diversi.
Riferimento D. Taverna, C. Mignogna, G. Santise, M. Gaspari, G. Cuda, “On-Tissue Hydrogel-Mediated Non-Destructive Proteomic Characterization: Application to fr/fr and FFPE Tissues and Insights for Quantitative Proteomics using a case of Cardiac Myxoma.” Proteomics Clin Appl. Nov 2:e1700167. 2018 D. Taverna, C. Mignogna, C. Gabriele, G. Santise, G. Donato, G. Cuda, and M. Gaspari, Anal. Bioanal. Chem., 409, 11, 2919–2930, 2017. |
Glicoproteomica
|
L'arricchimento di specifiche sottoclassi del proteoma sierico può permettere il rilevamento di proteine presenti a bassa concentrazione: le "low-abundance proteins".
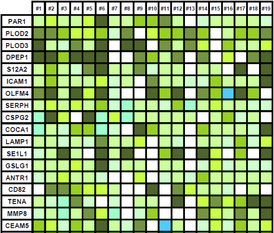
L'arricchimento di glicopeptidi da un digerito triptico può essere effettuato mediante metodica SPEG o TiO2. Attraverso questo step di purificazione, abbiamo rilevato proteine presenti nel siero a concentrazioni inferiori a 10 ng/mL: una soglia al di sotto della quale, è da molti ritenuto, si potrebbero trovare potenziali marcatori tumorali. Riferimenti C. Gabriele, F. Cantiello, A. Nicastri, F. Crocerossa, G.I. Russo, A. Cicione, M.D. Vartolomei, M. Ferro, G. Morgia, G. Lucarelli, G. Cuda, R. Damiano, M. Gaspari, “High-throughput detection of low abundance sialylated glycoproteins in human serum by TiO2 enrichment and targeted LC-MS/MS analysis: application to a prostate cancer sample set.” Anal Bioanal Chem. Jan;411(3):755-763, 2019. A. Nicastri, M. Gaspari, R. Sacco, L. Elia, C. Gabriele, R. Romano, A. Rizzuto, and G. Cuda, “N-Glycoprotein Analysis Discovers New Up-Regulated Glycoproteins in Colorectal Cancer Tissue,” J. Proteome Res., 13, 11, 4932–4941, 2014. |
Collaborazioni
|
Proteomics-UMG ha fornito supporto e tecnologia a collaboratori interni ed esterni all'Università Magna Graecia (UMG) interessati ad applicare l'analisi proteomica ai loro specifici interessi di ricerca. Le collaborazioni hanno riguardato lo studio di modifiche post-tradizionali di proteine, studi di interazione proteina-proteina, e proteomica cellulare e sub-cellulare.
Riferimenti principali J.G. Smith, S.G. Aldous, C. Andreassi, G. Cuda, M. Gaspari, A. Riccio, “Proteomic analysis of S-nitrosylated nuclear proteins in rat cortical neurons.” Sci Signal. vol. 11, no. 537, pii: eaar3396 Jul 2018. A. Pisano, S. Ceglia, C. Palmieri, E. Vecchio, G. Fiume, A. de Laurentiis, S. Mimmi, C. Falcone, E. Iaccino, A. Scialdone, M. Pontoriero, F. F. Masci, R. Valea, S. Krishnan, M. Gaspari, G. Cuda, G. Scala, and I. Quinto, “CRL3 IBTK Regulates the Tumor Suppressor Pdcd4 through Ubiquitylation Coupled to Proteasomal Degradation,” J. Biol. Chem., vol. 290, no. 22, pp. 13958–13971, May 2015. F. Bernaudo, F. Monteleone, M. Mesuraca, S. Krishnan, E. Chiarella, S. Scicchitano, G. Cuda, G. Morrone, H. M. Bond, and M. Gaspari, “Validation of a novel shotgun proteomic workflow for the discovery of protein-protein interactions: Focus on ZNF521,” J. Proteome Res., 14, 4, 1888–1899, 2015. E. Janda, C. Palmieri, A. Pisano, M. Pontoriero, E. Iaccino, C. Falcone, G. Fiume, M. Gaspari, M. Nevolo, E. Di Salle, A. Rossi, A. De Laurentiis, A. Greco, D. Di Napoli, E. Verheij, D. Britti, L. Lavecchia, I. Quinto, and G. Scala, “Btk regulation in human and mouse B cells via protein kinase C phosphorylation of IBtk gamma,” Blood, vol. 117, no. 24, pp. 6520–6531, Jun. 2011. |